 附图。图自越通社
附图。图自越通社
越南卫生部与世界卫生组织于8月4日上午联合举行视频研讨会,咨询专家关于临床试验数据核查和批准新冠疫苗紧急使用的意见。
这是该两个机构组织的首场会议,吸引韩国食品药品安全部(MFDS)和内外专家代表参加,意在协助越南制定国产新冠疫苗的3期临床试验计划。
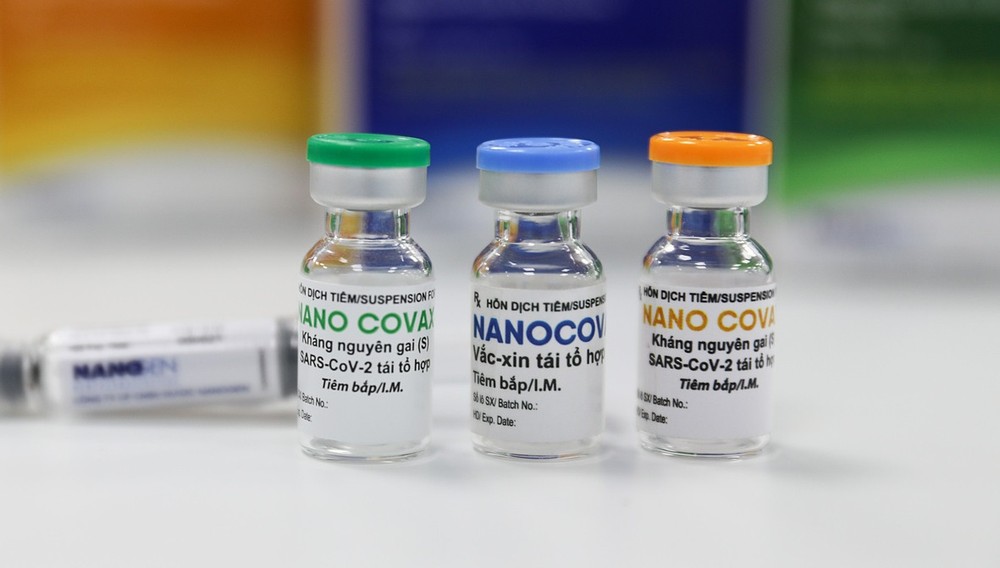
越南卫生部副部长、新冠疫苗临床试验和研发特别工作组组长陈文舜表示,目前,越南有两款候选疫苗已进入二期和三期临床试验阶段。越南正考虑为Nano Covax疫苗发放紧急使用许可。越南希望借鉴专家在疫苗研发和临床试验领域,尤其是发放疫苗紧急使用许可方面的经验。
越南卫生部科技与培训局副局长阮吴光博士表示,目前,Nano Covax 和 Covivac两款国产候选疫苗已进入二期和三期临床试验阶段。
具体是,由药用生物技术有限责任公司(Nanogen)与军医学院联合研发的Nano Covax疫苗正开展三期临床试验,目前正在评估安全性、免疫原性和对 18 岁以上越南志愿者的保护效力等3 个要素。
其中, 3a期1000名志愿者已完成Nano Covax新冠疫苗第二针接种,并进行安全性、免疫原性的中期评估,按6:1比例随机分配疫苗和安慰剂。3a期1.2万名志愿者按照2:1的比例随机分配疫苗和安慰剂,接种剂量分别为25mcg。
按计划,8月7日将对二期的最终结果进行总体评估;8月15日前将进行3a临床试验结果评价,其后,有关部门将审查3a期有关疫苗免疫原性和保护效力的初步数据。
对于由越南疫苗与医用生物制品研究院(IVAC)研发的新冠疫苗Covivac,研究小组正对一期人体临床试验的免疫原性进行评估,以便进入二期。研究小组希望第三季度末第四季度初将得出二期评估结果,以便进入三期。
对于疫苗生产技术转让问题,阮吴光博士透露,卫生部现已批准ARCT-154新冠疫苗的临床试验方案。这是由一家越南公司从美国购买的mRNA技术生产的疫苗。按计划,8月8日,研究团队将启动该疫苗的临床试验计划。
此外,越南已同俄罗斯和日本签署了2项新冠疫苗技术转让合同,相关工作正在进行中。
世界卫生组织建议越南制定国产疫苗和进口疫苗的使用和紧急使用实施细则。此外,世界卫生组织建议越南继续咨询国内外专家的意见,以便促进疫苗紧急使用,同时减少疫苗研发过程中的风险。
世界卫生组织(WHO)驻越南代表朴启东(Kidong Park)强调,在本次会议之后,双方将继续举行相关会议,旨在协助越南提升疫苗研发能力,加快国产疫苗批准和研发实施细则等的制定进程,为越南人民提供服务,并将越南国产疫苗推向国际市场。(越通社/民族与山区画报)





























